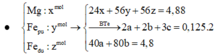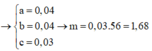Hoà tan hết 12,4 gam Fe,Cu,Fe2O3,CuO vào dung dịch H2SO4 đặc thu được dung dịch Y và 2,8 lít SO2. Cho dung dịch Y tác dụng với dung dịch NaOH dư, lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được chất rắn Z. Tính khối lượng của chất rắn Z

Những câu hỏi liên quan
Cho 4,88 gam hỗn hợp Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn X gồm ba kim loại và dung dịch Y gồm hai muối. Đun nóng X với dung dịch H2SO4 đặc, dư thu được 2,8 lít khí SO2 (đktc). Cho dung dịch NaOH dư vào Y, lọc lấy kết tủa rồi nung trong không khí, thu được 4,8 gam oxit. Giả thiết các phản ứng xảy ra hoàn toàn. Khối lượng của Fe trong X là: A. 1,68 gam. B. 2,80 gam. C. 1,12 gam. D. 2,24 gam.
Đọc tiếp
Cho 4,88 gam hỗn hợp Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn X gồm ba kim loại và dung dịch Y gồm hai muối. Đun nóng X với dung dịch H2SO4 đặc, dư thu được 2,8 lít khí SO2 (đktc). Cho dung dịch NaOH dư vào Y, lọc lấy kết tủa rồi nung trong không khí, thu được 4,8 gam oxit. Giả thiết các phản ứng xảy ra hoàn toàn. Khối lượng của Fe trong X là:
A. 1,68 gam.
B. 2,80 gam.
C. 1,12 gam.
D. 2,24 gam.
Hoà tan 10 gam hỗn hợp bột Fe và
F
e
2
O
3
bằng dung dịch
H
2
S
O
4
loãng dư thu được 0,672 lít khí (đktc) và dung dịch X. Cho dung dịch X tác dụng vài NaOH dư, thu được kết tủa. Nung kết tủa trong không khí đến khối lượng không đổi được 11,2 gam chất rắn. Thể tích dung dịch
K
M
n
O...
Đọc tiếp
Hoà tan 10 gam hỗn hợp bột Fe và F e 2 O 3 bằng dung dịch H 2 S O 4 loãng dư thu được 0,672 lít khí (đktc) và dung dịch X. Cho dung dịch X tác dụng vài NaOH dư, thu được kết tủa. Nung kết tủa trong không khí đến khối lượng không đổi được 11,2 gam chất rắn. Thể tích dung dịch K M n O 4 0,1M cần phản ứng vừa đủ với dung dịch X là
A. 180 ml
B. 60 ml
C. 100 ml
D. 120 ml
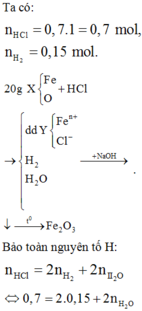
Cho 20 gam hỗn hợp X gồm Fe, FeO, Fe3O4, Fe2O3 tan vừa hết trong 700 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc kết tủa và nung trong không khí đến khối lượng không đổi được chất rắn Y. Khối lượng của Y là: A. 16 gam. B. 32gam. C. 8gam. D. 24gam.
Đọc tiếp
Cho 20 gam hỗn hợp X gồm Fe, FeO, Fe3O4, Fe2O3 tan vừa hết trong 700 ml dung dịch HCl 1M thu được 3,36 lít H2 (đktc) và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc kết tủa và nung trong không khí đến khối lượng không đổi được chất rắn Y. Khối lượng của Y là:
A. 16 gam.
B. 32gam.
C. 8gam.
D. 24gam.
hòa tan 1,44 gam hỗn hợp gồm Mg, Fe, Cu trong dung dịch H2SO4 đặc nóng thu được 0,784 lít SO2 và dung dịch X. Cho dung dịch X phản ứng với dung dịch NAOH dư , lọc lấy kết tủa đem nung trong không khí đên khối lượng không đổi thu được m gam chất rắn. Gía trị cảu m là:
CT chung A+2nH2SO4-->A2(SO4)n+nSO2+2nH2O
0.035/n 0.035 (mol)
A2(SO4)n-->A2On
0.035/n 0.035/n
mr=mA+(0.035/n)*n*16=2g
trắc nghiệm nSO42-=nSO2=0.035
BTĐT( chất rắn nên tự luận ko ghi được):nO2-=nSO42-=0.035
mr=mA+mO2-=2
Đúng 0
Bình luận (0)
A+2nH2SO4-->A2(SO4)n+nSO2+2nH2O
0.035/n 0.035 (mol)
A2(SO4)n-->A2On
0.035/n 0.035/n
mr=mA+(0.035/n)*n*16=2g
trắc nghiệm nSO42-=nSO2=0.035
BTĐT( chất rắn nên tự luận ko ghi được):nO2-=nSO42-=0.035
mr=mA+mO2-=2
#GG
Đúng 0
Bình luận (0)
CT chung A+2nH2SO4-->A2(SO4)n+nSO2+2nH2O
0.035/n 0.035 (mol)
A2(SO4)n-->A2On
0.035/n 0.035/n
mr=mA+(0.035/n)*n*16=2g
trắc nghiệm nSO42-=nSO2=0.035
BTĐT( chất rắn nên tự luận ko ghi được):nO2-=nSO42-=0.035
mr=mA+mO2-=2
Đúng 0
Bình luận (0)
Hòa tan hết hỗn hợp X gồm Fe, FeS, Fe3O4 trong dung dịch H2SO4 đặc, nóng (dư) thu được dung dich Y có khối lượng giảm 48 gam và 38,08 lít SO2 (đktc). Cho Y tác dụng với dung dịch NaOH (dư), lấy kết tủa rồi nung trong không khí đến khối lượng không đổi còn 64 gam chất rắn Z. Tính phần trăm theo khối lượng của Fe trong X? A. 68% B. 73,68% C. 43,18% D. 54%
Đọc tiếp
Hòa tan hết hỗn hợp X gồm Fe, FeS, Fe3O4 trong dung dịch H2SO4 đặc, nóng (dư) thu được dung dich Y có khối lượng giảm 48 gam và 38,08 lít SO2 (đktc). Cho Y tác dụng với dung dịch NaOH (dư), lấy kết tủa rồi nung trong không khí đến khối lượng không đổi còn 64 gam chất rắn Z. Tính phần trăm theo khối lượng của Fe trong X?
A. 68%
B. 73,68%
C. 43,18%
D. 54%
Đáp án B
nSO2 = 1,7 (mol)
Chất rắn Z là Fe2O3, nFe2O3 = 0,4 (mol)
2Febđ → Fe2O3
0,8 ← 0,4 (mol)
Ta có: mX = 1,7 ×64 – 48=60,8 (gam)
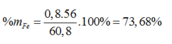
Đúng 0
Bình luận (0)
Cho 7,36 gam hỗn hợp X gồm Mg và Fe vào dung dịch chứa AgNO3 và Cu(NO3)2 khi phản ứng kết thúc thu được chất rắn Y và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 đặc nóng dư thu được 5,04 lít khí SO2 đktc (là sản phẩm khử duy nhất). Cho dung dịch NaOH dư vào Z được kết tủa T. Nung T trong không khí đến khối lượng không đổi được 7,2 gam hỗn hợp rắn. Phần trăm khối lượng của Fe trong X là: A. 38,04% B. 83,7% C. 60,87% D. 49,46%
Đọc tiếp
Cho 7,36 gam hỗn hợp X gồm Mg và Fe vào dung dịch chứa AgNO3 và Cu(NO3)2 khi phản ứng kết thúc thu được chất rắn Y và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 đặc nóng dư thu được 5,04 lít khí SO2 đktc (là sản phẩm khử duy nhất). Cho dung dịch NaOH dư vào Z được kết tủa T. Nung T trong không khí đến khối lượng không đổi được 7,2 gam hỗn hợp rắn. Phần trăm khối lượng của Fe trong X là:
A. 38,04%
B. 83,7%
C. 60,87%
D. 49,46%
Đáp án C

- Giả sử Mg, Fe đều phản ứng hết với muối kim loại => Z chứa toàn bộ số mol Mg2+ ; Fex+
=> T chứa Mg(OH)2 và Fe(OH)x => Chất rắn cuối cùng là MgO và Fe2O3 chắc chắn phải có khối lượng lớn hơn lượng kim loại ban đầu trong X => Không thỏa mãn đề bài (7,2 < 7,36)
=> Các muối nitrat phản ứng hết, kim loại dư và đó là Fe (vì Mg phản ứng trước)
=> kết tủa Y gồm Cu, Ag, Fe.
- Gọi nMg = a ; nFe(pứ) = b ; nFe dư = c => mX = 24a + 56b + 56c = 7,36 (1)
- Bảo toàn e cho phản ứng trao đổi muối: 2nMg + 2nFe pứ = nAg + 2nCu = 2a + 2b
- Khi Y + H2SO4 đặc nóng (Fe → Fe3+)
Bảo toàn electron: 2nCu + nAg + 3nFe dư = 2nSO2 = 2.5,04/22,4 = 0,45 mol
=> 2a + 2b + 3c = 0,45 (2)
- Như đã phân tích ở trên. chất rắn cuối cùng gồm MgO và Fe2O3.
Bảo toàn nguyên tố: nMg = nMgO = a ; nFe2O3 = ½ nFe pứ = 0,5b
=> mrắn = mMgO + mFe2O3 = 40a + 160.0,5b = 40a + 80b = 7,2 (3)
Từ (1,2,3) => a = 0,12 ; b = 0,03 ; c = 0,05 mol
=> mFe(X) = 56.(0,03 + 0,05) = 4,48g
=> %mFe(X) = 4,48: 7,36 = 60,87%
Đúng 0
Bình luận (0)
1.cho hỗn hợp gồm 1,8.1022nguyên tử Fe,24g Fe2O3 và 23,2g Fe3O4 tác dụng hết với dung dịch H2SO4 loãng thu được dung dịch A.Cho dung dịch A tác dụng với dung dịch NaOH dư,lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được m g chất rắn Ca)lập pthh b)tính m2.Cho 14,6g hỗn hợp 3 kim loại Cu Al Fe tác dụng với HCl dư thu được 7,48l H2(đktc),m g hỗn hợp muối và 6,4g chất rắn không tana)lập pthh b)tính m ,thành phần % về khối lượng của mỗi kim loại trong hỗn hợp kim loại trên
Đọc tiếp
1.cho hỗn hợp gồm 1,8.1022nguyên tử Fe,24g Fe2O3 và 23,2g Fe3O4 tác dụng hết với dung dịch H2SO4 loãng thu được dung dịch A.Cho dung dịch A tác dụng với dung dịch NaOH dư,lọc kết tủa đem nung trong không khí đến khối lượng không đổi thu được m g chất rắn C
a)lập pthh b)tính m
2.Cho 14,6g hỗn hợp 3 kim loại Cu Al Fe tác dụng với HCl dư thu được 7,48l H2(đktc),m g hỗn hợp muối và 6,4g chất rắn không tan
a)lập pthh b)tính m ,thành phần % về khối lượng của mỗi kim loại trong hỗn hợp kim loại trên
Cho 8 gam hỗn hợp A gồm Mg và Fe tác dụng hết với 200 mL dung dịch CuSO4 đến khi phản ứng kết thúc, thu được 12,4 gam chất rắn B và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc và nung kết tủa ngoài không khí đến khối lượng không đổi thu được 8 gam hỗn hợp gồm 2 oxit. Thể tích NO thoát ra khi hoà tan B trong dung dịch HNO3 dư là A. 1,12 lít. B. 3,36 lít C. 4,48 lít D. 6,72 lít
Đọc tiếp
Cho 8 gam hỗn hợp A gồm Mg và Fe tác dụng hết với 200 mL dung dịch CuSO4 đến khi phản ứng kết thúc, thu được 12,4 gam chất rắn B và dung dịch D. Cho dung dịch D tác dụng với dung dịch NaOH dư, lọc và nung kết tủa ngoài không khí đến khối lượng không đổi thu được 8 gam hỗn hợp gồm 2 oxit. Thể tích NO thoát ra khi hoà tan B trong dung dịch HNO3 dư là
A. 1,12 lít.
B. 3,36 lít
C. 4,48 lít
D. 6,72 lít
Hỗn hợp B gồm Cu và Fe dư. nCu = 0,15 mol; nFe = 0,1 - 0,05 = 0,05 mol.
Khi tác dụng với dung dịch HNO3: Theo phương pháp bảo toàn eletron
Chất khử là Fe và Cu
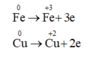
Chất oxi hoá là HNO3
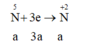
Ta có 3a = 0,15 + 0,3; a = 0,15 (mol),
VNO = 0,15.22,4 = 3,36 (lít)
Đáp án B
Đúng 0
Bình luận (0)
Hòa tan hết 15,2 gam Fe, Cu bằng dung dịch H,SO, đặc nóng sau phản ứng thu được dung dịch X. Cho X tác dụng với NaOH dư thu được kết tủa Y. Nung Y ngoài không khí đến khối lượng không đổi thu được 20,8 gam hỗn hợp Fe,O,, CuO. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu?
\(2Fe+6H_2SO_4\to Fe_2(SO_4)_3+3SO_2\uparrow+6H_2O\\ Cu+2H_2SO_4\xrightarrow{t^o}CuSO_4+SO_2\uparrow+2H_2O\\ Fe_2(SO_4)_3+6NaOH\to 2Fe(OH)_3\downarrow+3Na_2SO_4\\ CuSO_4+2NaOH\to Cu(OH)_2\downarrow+Na_2SO_4\\ 2Fe(OH)_3\xrightarrow{t^o}Fe_2O_3+3H_2O\\ Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\)
Đặt \(n_{Cu}=x(mol);n_{Fe}=y(mol)\Rightarrow 64x+56y=15,2(1)\)
Theo các PT: \(n_{Fe_2O_3}=0,5y(mol);n_{CuO}=x(mol)\)
\(\Rightarrow 80x+80y=20,8(2)\\ (1)(2)\Rightarrow x=0,08(mol);y=0,18(mol)\\ \Rightarrow \%_{Cu}=\dfrac{0,08.64}{15,2}.100\%=33,68\%\\ \Rightarrow \%_{Fe}=100\%-33,68\%=66,32\%\)
Đúng 2
Bình luận (0)